바이오파마(Bio Farma)사 신규 장티푸스 접합 백신 Bio-TCV®, 인도네시아에서 사용승인 받아
바이오파마(Bio Farma)사 신규 장티푸스 접합 백신 Bio-TCV®, 인도네시아에서 사용승인 받아
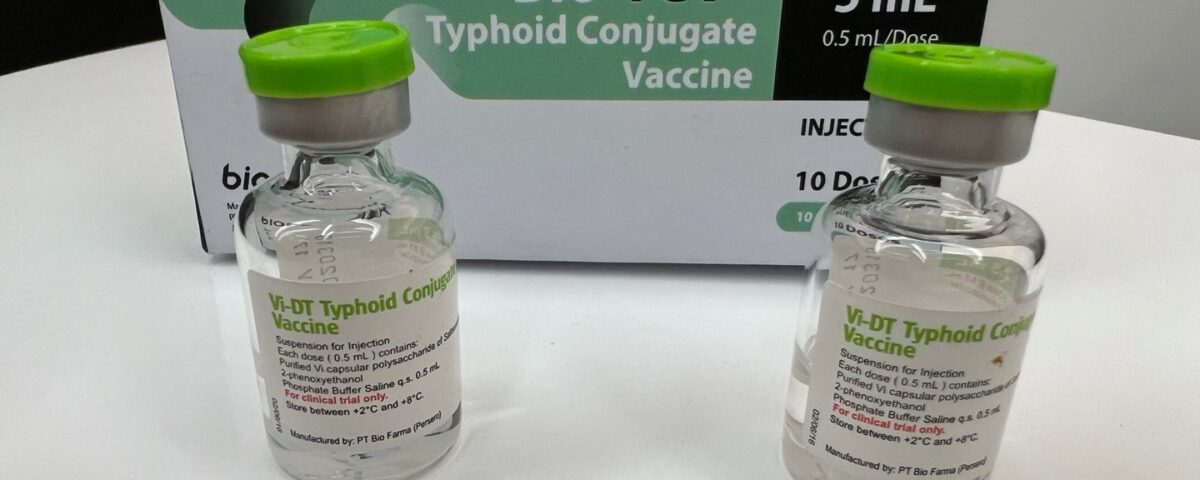
Bio-TCV® Vi-DT typhoid conjugate vaccine, developed at IVI and technology-transferred to Bio Farma, was licensed by BPOM, Indonesia’s regulatory authority. Credit: Bio Farma
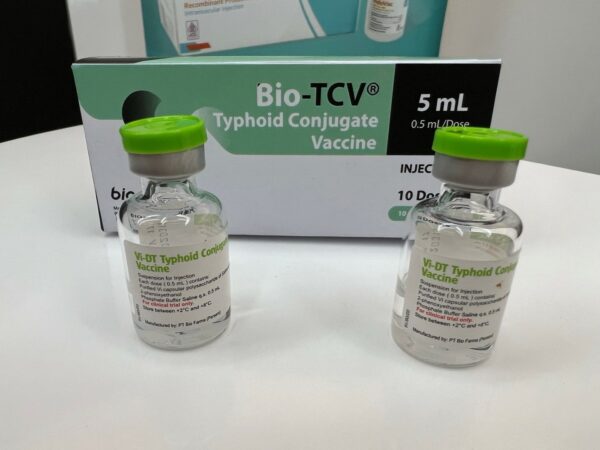
IVI가 개발하여 바이오파마에 기술 이전한 Bio-TCV® Vi-DT 장티푸스 접합 백신이 인도네시아 규제기관인 BPOM으로부터 사용허가를 획득하였다. (사진=바이오파마)
국제백신연구소(IVI)와 인도네시아 생명공학회사인 바이오파마(Bio Farma)는 바이오파마사의 Bio-TCV® 장티푸스 접합 백신(TCV)이 인도네시아 국가의약품관리청(BPOM)으로부터 사용승인을 획득하고 이어 시판 허가도 받았다고 발표했다.
Bio-TCV®는 디프테리아 독소 운반 단백질에 접합된 Vi 다당체(Vi-DT) 백신으로, IVI가 최초 개발하여 2014년 바이오파마에 기술 이전하였다. 이 장티푸스 백신 공동 개발 사업의 범위에는 처음부터 비임상 개발과 임상 1~3상 시험, 현지 사용승인 획득 및 WHO 사전승인(PQ) 신청을 위한 IVI의 기술 지원이 포함되어 있었다. WHO 사전승인을 받아야 유니세프, WHO 등 UN기구나 세계백신면역연합(Gavi)과 같은 지원 기관이 백신을 구입하여 세계공중보건에 사용할 수 있다. 안전하고 효과적이며 저렴한 TCV를 개발하기 위해 10여년 간 이어진 협력 파트너십은 빌앤멜린다게이츠재단의 일부 연구비 지원으로 이루어진 것이다.
IVI의 임상 및 규제 담당 사무차장대행 수샨트 사하스트라부디(Sushant Sahastrabuddhe) 박사는 “바이오파마와 함께 Bio-TCV®의 현지 사용승인 획득 소식을 전하게 되어 기쁘다. 이는 10년간 협력 관계의 성과가 실현된 중요한 결실”이라면서, 이 백신 개발 프로그램의 예산을 지원해 준 빌앤멜린다게이츠 재단과 파트너십에 동참해온 인도네시아 내 협력기관들에 감사를 표했다. 그는 또 “기후변화 및 항생제 내성 증가가 장티푸스의 유병률과 중증도에 영향을 미치고 있다는 증거가 점차 늘고 있는 이 시점에서 백신은 장티푸스를 통제할 수 있는 핵심적인 수단”이라면서, “이제 우리는 Bio-TCV®가 WHO 사전승인을 통과하여 글로벌 백신 시장에 도입되기를 기대하고 있다”고 밝혔다.
바이오파마의 샤디크 아카샤(Shadiq Akasya) 사장은 “IVI와의 긴밀한 협력을 통해 바이오파마는 장티푸스 접합 백신(Bio-TCV®)를 성공적으로 개발할 수 있었다”면서, “이 백신의 인도네시아 국가의약품관리청(BPOM) 사용 승인으로 자사 백신 포트폴리오에 또 하나의 제품이 추가되었다”고 밝혔다. 그는 “Bio-TCV®는 생후 9개월부터 장티푸스 감염을 예방할 수 있는 중요한 수단이 될 것으로 확신한다”면서, “Bio-TCV®의 성공적인 개발은 국제 품질 표준을 준수하는, 안전하고 효과적인 백신 공급을 통해 감염병을 퇴치하고자 하는 바이오파마의 세계보건에 대한 의지를 웅변하는 것”이라고 말했다.
게이츠재단의 장감염 백신 부문 전략 수석인 던컨 스틸(Duncan Steele) 박사는 “인도네시아에서 Bio-TCV®의 사용 승인을 축하한다”면서, “이는 바이오파마의 승인받은 백신제품 목록에 또 하나의 이정표가 되며, 공중보건용 백신의 개발을 위한 파트너십의 또 다른 성공 사례다. 이 기술을 개발하고 바이오파마에 이전하는 데 있어 보여준 IVI의 리더십은 두 기관 모두의 공로가 된다”고 말했다.
IVI와 바이오파마는 인도네시아 3개 주요 도시에서 수행된 임상 3상 시험을 통해 1회투여 Vi-DT의 안전성과 면역원성 및 WHO 사전승인을 받은 TCV 대조군에 대한 비열등성을 확인한 바 있다. 인도네시아 국가의약품관리청은 이러한 시험 결과를 토대로 인도네시아 내 9개월~45세 인구집단에 대한 백신 사용을 허가하였다. 바이오파마는 WHO 사전승인 신청서를 제출할 예정이며, 승인을 획득하면 글로벌 공중보건 시장에 저렴한 신규 TCV가 추가 도입되어 세계백신면역연합(Gavi)을 통해 저소득국가에 보급될 것으로 기대된다.
장티푸스는 장티푸스균 감염으로 인해 발생하며 생명을 위협할 수 있는 질병으로 특히 소아와 젊은 성인에서 자주 발병한다. WHO에 따르면 연간 1100~2000만 명이 감염되는 것으로 추정되며, 대체로 중저소득국가에서 감염률이 높다. 백신접종이 장티푸스를 통제할 수 있는 효과적인 예방 전략인 것으로 밝혀졌으나, 현재 WHO의 사전승인을 받은 백신은 단 2종뿐이다. IVI는 공중보건 시장에서 사용될 수 있는 TCV의 다양화를 위해 전 세계 백신 제조사들과 지속적으로 협력하고 있다.
###
바이오파마(Bio Farma)
PT Bio Farma(페르세로) 또는 “바이오파마”는 인도네시아의 국영 백신 및 항혈청제제 제조업체다. 올해로 창립 133주년을 맞이한 바이오파마는 연간 32억 회분 이상의 백신을 생산 및 유통하는 국제적으로 인정받는 생명과학 기업으로 성장했다. 바이오파마는 동남아시아에서 가장 큰 백신 제조업체로서, 인도네시아의 확대 예방접종 프로그램(EPI) 수요뿐만 아니라 150개 이상의 국가에 글로벌 시장을 공급하고 있다. 바이오파마가 글로벌 시장에 진출할 수 있었던 것은 다수의 백신이 세계보건기구(WHO)로부터 사전적격성평가 인증(PQ)을 획득했기 때문이다. 빌앤멜린다게이츠재단(BMGF)과 미국의 글로벌보건 기관인 PATH는 바이오 파마와 협력하여 글로벌 소아마비 퇴치 이니셔티브(GPEI)를 지원하기 위해 새로운 경구용 소아마비 백신 2형(nOPV2)을 생산했으며, 이는 2020년에 WHO로부터 최초의 긴급사용목록(EUL) 백신으로 등재되었다.
바이오파마는 먼 미래 세대까지 그 존재가 유지되는 건강한 국가를 만드는 데 중요한 역할을 하고 있으며, “삶의 질 향상에 헌신한다”는 철학을 바탕으로 글로벌 보건안보 증진에 전념하고 있다. 2020년 초에는 바이오파마를 모회사로 하는 인도네시아 국영 제약 지주회사가 설립되었다. 이 지주회사의 설립은 인도네시아 국가 제약산업의 자립을 강화하고 제약 생태계를 지원하는 제품의 가용성을 높이는 것을 목표로 한다. 자세한 내용은 www.biofarma.co.id 참조
국제백신연구소 IVI
국제백신연구소(IVI)는 세계 공중보건을 위해 안전하며 효과적이고 저렴한 백신의 발굴 개발 보급에 전념하는 비영리 국제기구이자 대한민국에 본부를 둔 최초의 국제기구다. 현재 IVI는 콜레라, 장티푸스, 치쿤구니아, 살모넬라, 주혈흡충증, E형간염, 인유두종바이러스, 코로나19 등에 대한 백신의 연구개발을 전임상부터 임상시험까지 전 단계에 걸쳐 시행하고 있으며, 아시아 아프리카 남미 등 세계 30여개 국가에서 활동하고 있다. IVI는 세계 최초의 저가 경구용 콜레라 백신을 개발하여 WHO 사전승인을 받았으며, 차세대 장티푸스 접합백신을 개발하여 WHO 사전승인 획득이 추진되고 있다.
1997년 유엔개발계획(UNDP)의 주도로 설립된 IVI는 현재 UN과는 분리된 독립적 국제기구로 운영되고 있으며, 대한민국, 스웨덴, 인도, 핀란드, 태국 등 운영비 공여국을 포함하여 세계 39개국과 세계보건기구(WHO)가 IVI설립협정 회원국으로 참여하고 있다. 서울대학교 연구공원에 본부를, 스웨덴에 유럽 지역사무소를 개소하였으며, 가나 에티오피아 마다가스카르에 협력센터를 운영하고 있다. 자세한 정보는 www.ivi.int 참조.
관련문의
국제백신연구소(IVI) 공보관 변태경
전화: 02-881-1159
휴대폰: 010-8773-6071
이메일: tkbyun@ivi.int


